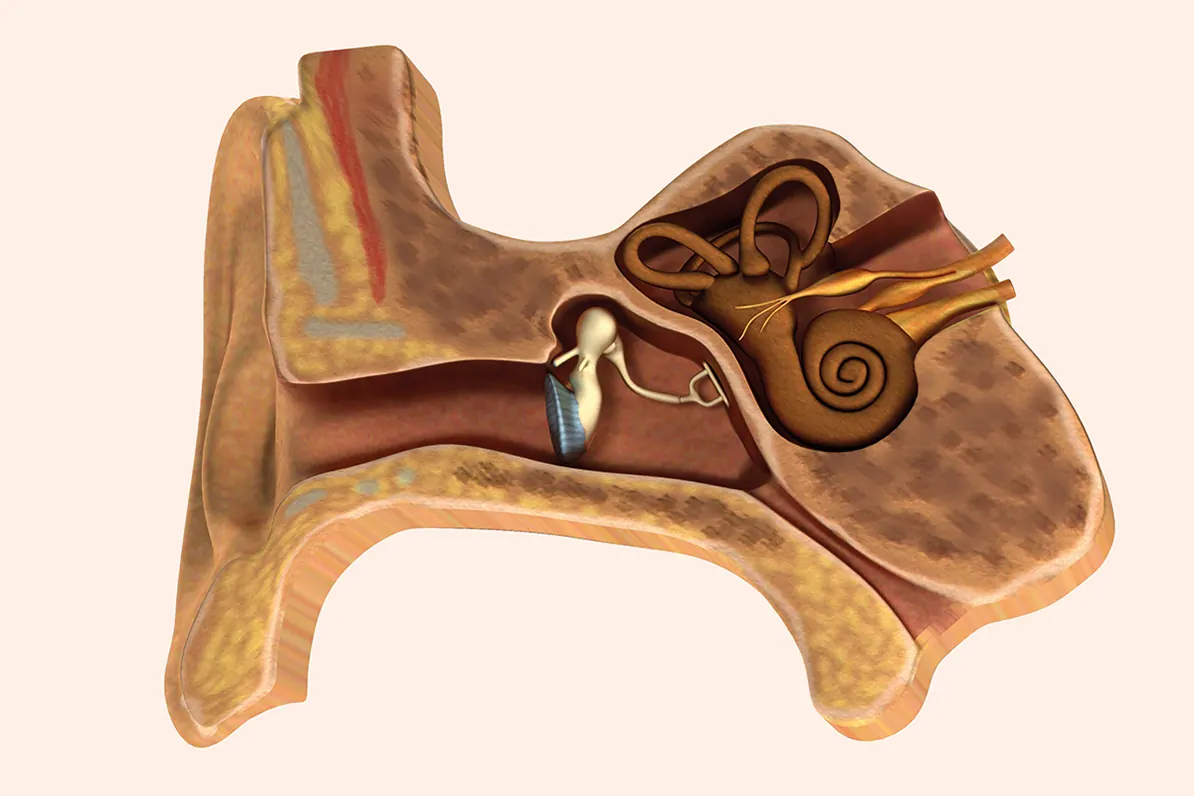
Ototoxicidad en el cáncer infantil
El tratamiento de muchos cánceres infantiles se realiza con cisplatino o carboplatino, unos fármacos considerados ototóxicos por los efectos secundarios que producen y entre los que cabe destacar la pérdida de audición y los tinnitus. Estos efectos comienzan a manifestarse durante el tratamiento, pero pueden prolongarse hasta varios años después de haberlo finalizado. La pérdida de la audición puede dificultar el rendimiento escolar y la socialización del niño, especialmente durante los primeros años de vida. La realización de una valoración previa al tratamiento y una monitorización durante y al final del mismo, puede contribuir a mejorar la calidad de vida de estos pacientes una vez superada la enfermedad.
Ciertos medicamentos quimioterapéuticos (cisplatino, carboplatino) y antimicrobianos (gentamicina, tobramicina, vancomicina y amikacina) son tóxicos para las estructuras del oído interno y pueden causar acúfenos, pérdida de audición y disfunción vestibular. Estos efectos secundarios, denominados «ototoxicidad», pueden disminuir la calidad de vida psicosocial, física y general de los pacientes, y aparecer durante o después del tratamiento.

Los agentes de platino (cisplatino y carboplatino) han mejorado las tasas de curación de muchos cánceres infantiles, pero su uso puede provocar pérdida auditiva neurosensorial irreversible de alta frecuencia. El déficit es progresivo al aumentar la dosis acumulativa de cisplatino.
Las conclusiones, en cuestión de tasas de afectación, de algunos estudios científicos sobre ototoxicidad en la población pediátrica sometida a estos tratamientos determinan que «aproximadamente el 50% de los niños tratados con regímenes basados en cisplatino desarrollan algún grado de pérdida auditiva permanente. En altas dosis, hasta el 90% de los niños pequeños pueden sufrir déficits de moderados a severos, con una pérdida auditiva grave hasta en un 25% de los casos».
La patología del oído inducida por radiación puede afectar a todas las partes del sistema auditivo. La radioterapia craneal, cuando se usa como una modalidad única, generalmente produce ototoxicidad solo cuando la dosis coclear supera los 32 Gy. La edad del paciente, si es especialmente joven, y la presencia de un tumor cerebral y/o hidrocefalia, pueden aumentar la susceptibilidad a la pérdida de audición.
El inicio de la hipoacusia asociada a la radiación puede ser gradual, manifestándose meses o incluso años después de la exposición.
Cuando se usa junto al cisplatino, la radioterapia puede agravar esta pérdida de audición asociada a los agentes quimioterápicos derivados del platino.
La susceptibilidad individual a la ototoxicidad del cisplatino es variable. Se ha demostrado que entre el 38-47% de la diferencia en los grados de susceptibilidad a la ototoxicidad inducida por cisplatino en las personas se debe a variables genéticas.
Además, se ha comprobado que los niños están más predispuestos a sufrir la ototoxicidad de los agentes derivados del platino que los adultos.
La toxicidad coclear del platino se produce a través de la interferencia con la transducción de señales del órgano de Corti en la cóclea.
Como consecuencia, se originan daños en tres estructuras concretas:
— Las células ciliadas externas (células efectoras).
— El ganglio espiral (suministro de nervio principal de la cóclea).
— La estría vascular (suministro de sangre primaria).

Las células ciliadas cocleares están dispuestas de tal manera que cada una es sensible a un rango de frecuencias limitado. El daño relacionado con la quimioterapia comienza en la células ciliadas externas de la base de la cóclea, donde se procesan los sonidos de alta frecuencia. Por lo tanto, el uso de compuestos de platino puede derivar en una pérdida auditiva neurosensorial bilateral, que inicialmente involucra las frecuencias más altas (≥8 kHz).
Con el aumento de las dosis acumulativas de quimioterapia o cuando se combinan con otros factores ototóxicos, como la irradiación antes de la quimioterapia, la pérdida de células ciliadas puede progresar apicalmente en la cóclea e involucrar la percepción del habla.
Algunos de los factores que determinan un mayor riesgo de hipoacusia por el uso de agentes de platino son:
— Una edad más joven.
— Una mayor dosis acumulativa de quimioterapia.
— Los tumores del sistema nervioso central (SNC).
— La radiación concomitante del SNC.

Otros factores que pueden contribuir a esta pérdida de audición asociada con agentes de platino, son medicamentos como los antibióticos aminoglucósidos y los diuréticos de ASA, utilizados como tratamientos complementarios.
Además, como complicación añadida puede aparecer una función renal deteriorada que retrase la excreción de los agentes de platino ototóxicos. Por último, la presencia de patologías del oído coexistentes, como otitis crónica, derrames del oído medio o acumulación de cerumen, pueden empeorar aún más la deficiencia auditiva.
El tiempo medio para la observación de la ototoxicidad, según lo evaluado por los criterios de ASHA (American Speech-Language-Hearing Association), es de 135 días. En este período de tiempo, ningún paciente mostró mejoría en la audición y la mayoría de las revisiones sugieren que la pérdida de audición es permanente y estable después de completar la terapia. En ocasiones, se han observado pérdidas auditivas progresivas hasta 136 meses después del final del tratamiento con compuestos de platino en pacientes pediátricos.
Pérdida auditiva en la infancia
La pérdida de audición en los niños puede afectar a la calidad de vida, al desarrollo socioemocional,
al rendimiento académico, al desarrollo psicosocial y a la adquisición del habla y del lenguaje. La identificación temprana de deficiencias auditivas es importante para facilitar la adquisición normal o casi normal de las habilidades del lenguaje, académicas y de afrontamiento, especialmente en niños.
En el caso de los pequeños sometidos a este tipo de tratamientos, la ototoxicidad pasa a un segundo o tercer plano. La vida prima sobre todas las cosas y los efectos colaterales que pudiese tener en la audición son un «mal menor» que, en muchos casos, hay que asumir.

Los programas de detección precoz y seguimiento en estos pacientes de riesgo no están generalizados en España. Con protocolos exhaustivos y técnicas de exploración que permitan el diagnóstico precoz, como son las Otoemisiones Acústicas por Productos de Distorsión (PD-Grama) o audiometrías de alta frecuencia (≥8 kHz), que facilitan una monitorización continuada en el tiempo de la afectación, se podría minimizar el impacto que pudiese tener una afectación progresiva en la audición.
Las emisiones otacústicas por productos de distorsión son una prueba muy útil para detectar los cambios en la función auditiva causados por la ototoxicidad, sobre todo en niños que no colaboran por su corta edad y a los que no se puede evaluar mediante audiometría tonal, o para aquellos cuyos resultados presenten una fiabilidad baja.
Respecto a la audiometría tonal de alta frecuencia, se manejan estadísticas muy elevadas de afectación. En más de un 80% de los niños estudiados se ha evidenciado pérdida auditiva, en su mayoría en frecuencias superiores a 8 kHz.
Es de especial importancia que los niños enfermos de larga duración, tras superar la enfermedad, vuelvan a recuperar la mayor normalidad en las rutinas de su vida, esforzándonos lo máximo posible en que las condiciones sean semejantes a las de los niños de su edad, y que la enfermedad tenga el menor impacto posible, minimizando sus secuelas; y esto, también es necesario, en lo relativo a la audición.
Por lo tanto, y bajo estas circunstancias, se debería concienciar sobre la importancia de la audición a los diferentes profesionales implicados en el tratamiento del niño oncológico y a sus familias, así como informar y formar sobre las implicaciones en el desarrollo de una correcta audición en la infancia frente a las consecuencias de su deterioro. A día de hoy, crear conciencia de la trascendencia que supone la implementación de la disciplina de la audiología en los pacientes oncológicos se convierte en una tarea pendiente de nuestro sistema de salud.
Referencias
Si deseas ampliar información, puedes consultar los siguientes artículos científicos:
Irany Paz, M., Codjambassis, D., & Pinto, J. (2000). Emisiones otoacústicas en la detección precoz de ototoxicidad inducida por cisplatino. RevOtorrinolaringol, 60, 7-13.
Toral-Martiñón, R., Poblano, A., Collado-Corona, M. A., & González, R. (2003). Efectos del cisplatino en la función auditiva en niños con cáncer. Evaluación por emisiones otoacústicas. GacMédMéx, 139(6).
American Speech-Language-Hearing Association. Audiologic management of individuals receiving cochleotoxic drug therapy. ASHA 1994; (suppl12) 36:11-9.
Autoras

DRA. Mª TERESA ALMELA
OTORRINOLARINGÓLOGA
Especialista en otorrinolaringología.
Hospital Universitario del Mar Menor.
Responsable de cirugía Clínica Templado.

SHEILA TEMPLADO
AUDIÓLOGA
Licenciada en Audiología por la Universidad de Coimbra.
Fundadora de Clínica Templado, especializada en la patología del oído y atención a pacientes con problemas de audición.