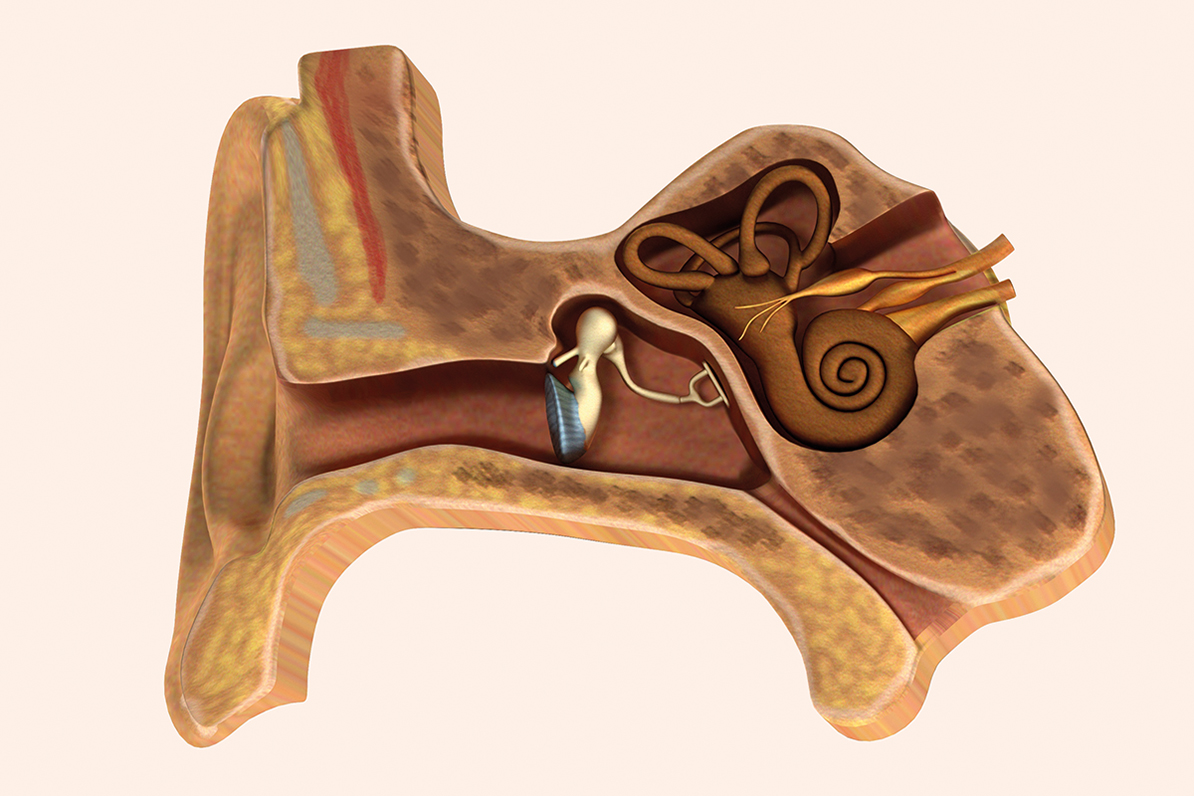
La otitis serosa se define como la acumulación de líquido en el oído medio con integridad de la membrana timpánica, en ausencia de signos y síntomas de infección aguda. Este líquido puede ser mucoso, seroso o una combinación de ambos, pudiendo variar en su composición a lo largo de la evolución de la enfermedad. La duración puede ser aguda (inferior a tres semanas), subaguda (de tres semanas a tres meses) o crónica (superior a tres meses). Es muy frecuente en la edad pediátrica, siendo en la mayor parte de los casos casi asintomática, diagnosticada de forma accidental en una exploración realizada por otra causa. En adultos es menos frecuente encontrarla de manera aislada.
Epidemiología
Afecta sobre todo a niños menores de 8 años. Se considera que aproximadamente el 70% de los niños tienen al menos un episodio de otitis serosa antes de los tres años.
Los factores de riesgo más conocidos para el desarrollo de esta enfermedad son la infección aguda de la vía aérea superior, la alergia nasal y la hipertrofia adenoidea, aunque existen muchos otros factores que influyen en su desarrollo.
Se considera que existe una susceptibilidad genética para padecer otitis serosa, en probable relación con factores anatómicos y fisiológicos.
Existen enfermedades congénitas que se asocian a una mayor frecuencia de otitis serosa.
Es más prevalente en varones, en niños en contacto con fumadores, en los que acuden a guarderías y en los alimentados con biberón frente a aquellos que reciben lactancia materna.
Patogenia
El hecho clave en el desarrollo de una otitis serosa es la disfunción de la trompa de Eustaquio. La función principal de la trompa consiste en equilibrar la presión del oído medio a la presión atmosférica, además del drenaje de la secreción de la mucosa y la protección del mismo.
Cuando la apertura de la trompa es insuficiente, se genera una presión negativa en el interior de la caja timpánica que favorece la aparición de un trasudado en un intento de compensar el desequilibrio de presiones.
Aproximadamente el 70% de los niños tienen al menos un episodio de otitis serosa antes de los tres años.
Si la obstrucción de la trompa es completa el líquido contenido en oído medio será el resultado del exudado producido por la mucosa y, por lo tanto, será estéril. Sin embargo, cuando dicha obstrucción es incompleta, con una apertura intermitente de la trompa, la presión negativa del oído medio puede succionar secreciones de la vía aérea superior, resultando un exudado con bacterias que pueden colonizar el oído medio e infectarlo, originando una otitis media aguda en el seno de una otitis serosa. Este hecho explica que los gérmenes aislados en una otitis serosa aguda sean característicamente aquellos que colonizan con más frecuencia la vía respiratoria superior.
El origen de la obstrucción tubárica puede deberse a causas mecánicas o funcionales. En la edad pediátrica es mucho más frecuente la obstrucción funcional, debido a la inmadurez de la trompa. En el niño, la trompa es de menor longitud y con una posición mucho más horizontalizada (10º de inclinación respecto a la horizontal frente a los 45º del adulto) que determina una mala función del músculo tensor del velo del paladar y por tanto una deficiente apertura de la trompa. Además el cartílago es de menor consistencia y con mayor facilidad para colapsarse.
La mucosa de la trompa puede ser objeto de una inflamación por afectación directa de un proceso alérgico o infeccioso, tanto vírico como bacteriano.
Los pacientes que padecen una alergia nasal son más susceptibles de desarrollar una otitis serosa, pero en la mayoría de los pacientes con otitis serosa no es posible identificar un mecanismo alérgico subyacente y hay pacientes con rinitis alérgica que nunca presentaran disfunción tubárica.
Se considera que existe una susceptibilidad genética para padecer otitis serosa, lo que explica también la diferencia de la prevalencia en función de la raza: mayor en indios americanos y esquimales.
Una infección bacteriana, tanto en nasofaringe como en oído medio, es capaz de desencadenar el mecanismo inflamatorio que determina una otitis serosa.
Se considera que existe mayor riesgo de cronicidad o de recurrencia en varones, de raza blanca, con un comienzo precoz de la otitis, que viven en un ambiente de fumadores, los que asisten a guardería y con mayor número de hermanos. También en aquellos con historia familiar de otitis.
En la edad adulta suele presentarse en el seno de una infección de vía respiratoria superior, en especial la rinosinusitis, o como persistencia de contenido seromucoso tras la resolución de una otitis media aguda.
Clínica
La mayoría de las veces se presenta de forma asintomática, siendo descubierta de forma casual o en el seguimiento tras una otitis media aguda.
El síntoma más comúnmente referido es la hipoacusia, que se instaura de forma lenta y progresiva de modo que pasa desapercibida tanto para el paciente como para sus padres y educadores, retrasando el diagnóstico. En el caso de los niños suele ser manifestada como disminución de la atención o del rendimiento escolar, o cambios en el comportamiento. Varios estudios demuestran que la pérdida auditiva es menor en los niños de menor edad.

El paciente puede referir sensación de plenitud ótica, ruidos, amplificación de sonidos propios (autofonía) y ajenos. En ocasiones puede producir otalgia leve, sobre todo a raíz de un proceso catarral, haciéndonos pensar en una sobreinfección los casos que se presentan con otalgia intensa. El diagnóstico diferencial de esta enfermedad respecto a la otitis media aguda se basa en la ausencia de síntomas infecciosos, tales como fiebre o malestar general.
Los síntomas suelen referirse de forma bilateral, al contrario de lo que ocurre en los adultos. Cuando se presenta de forma unilateral debe hacernos pensar en una tumoración en la nasofaringe, como un angiofibroma o una neoplasia maligna.
Puede acompañarse de sensación de mareo o acúfenos y, excepcionalmente, de una parálisis facial periférica provocada por el aumento de presión en oído medio en los casos en que el conducto de Falopio es dehiscente, y que se recupera tras el tratamiento.
La clínica suele ser menos clara en niños más pequeños en los que podemos encontrar solo irritabilidad y rechazo del alimento.


Diagnóstico
Exploración física.
La otoscopia es la prueba fundamental para el diagnóstico, siendo definitiva en una parte importante de los casos. Existen muchas anomalías en la membrana timpánica asociadas a la otitis serosa. Por lo general, muestra un tímpano íntegro, edematizado y opaco con un aumento de la vascularización radial, y puede estar en posición normal, abombado o retraído. En los procesos de corta evolución la coloración suele ser rojiza, generalmente con una membrana engrosada. Sin embargo en los casos crónicos el aspecto suele ser azulado, resultado del depósito de hemosiderina en el exudado, y la membrana suele estar adelgazada y atrófica, con tendencia a la retracción, pudiendo desencadenar en una otitis adhesiva. En los casos en que el tímpano conserva su transparencia, es posible observar en ocasiones niveles o burbujas (indicativo de que la trompa funciona parcialmente).
La otoscopia neumática puede ser una gran ayuda en el diagnóstico de la otitis serosa en los casos dudosos, al mostrar una membrana timpánica con menor movilidad. Constituye una exploración muy accesible y con una sensibilidad y especificidad respectivamente del 94% y 80% frente a la miringotomía, en manos expertas.
La acumetría puede servirnos de orientación en una primera valoración en niños colaboradores, poniendo de manifiesto una hipoacusia transmisiva en el contexto de una historia clínica y una imagen otoscópica compatibles.
Exploraciones complementarias
Timpanometría: es una prueba que traduce la complianza de la membrana timpánica, que se ve alterada cuando el oído medio se encuentra ocupado, sin embargo, no siempre es determinante.
Típicamente obtendremos una curva aplanada (curva tipo B) paralela al eje de abscisas, o con el punto de mayor compliancia desplazado hacia presiones negativas (curva tipo C).


También podemos encontrar este patrón en otras patologías de oído medio. Otros resultados posibles, aunque no típicos, son curvas de amplitud normal o, con menor frecuencia, desplazadas hacia presiones positivas.

Curvas Timpanométricas.
La audiometría generalmente muestra una hipoacusia de transmisión con un umbral diferencial en torno a los 20 dB, pero una otitis serosa por sí sola no justifica una pérdida mayor de 30 dB, que debe hacernos pensar en otras alteraciones del oído medio. Sirve además para detectar una posible afectación neurosensorial asociada al cuadro, determinada por el paso de mediadores inflamatorios al oído interno a través de la ventana redonda. Sin embargo, el papel de la audiometría en el diagnóstico de los niños es limitado debido a la dificultad para su correcta colaboración, siendo necesario en ocasiones recurrir a audiometrías de juego o con reflejos condicionados.
Evolución
La evolución natural de la otitis serosa en los niños es hacia la curación espontánea en un período de semanas a meses, en la mayoría de los casos. En los adultos, esta tendencia es menos marcada, por lo que el tratamiento debe ser más agresivo, pasando con más rapidez al drenaje quirúrgico, tras el fracaso inicial del tratamiento médico.
Los tímpanos que han padecido durante mucho tiempo de otitis serosa tienen tendencia a la atrofia, pudiendo producirse una perforación timpánica, bolsas de retracción, otitis adhesiva o, incluso, desarrollar un colesteatoma.
El riesgo de desarrollar una otitis serosa disminuye con el crecimiento del niño, fundamentalmente debido a la maduración de la trompa de Eustaquio y del sistema inmunitario.


Aproximadamente el 50% de los oídos con otitis serosa se normalizan en un período de dos meses, por lo que es recomendable esperar al menos tres meses antes de establecer un tratamiento quirúrgico. Sin embargo, la decisión de observación durante tiempos superiores a 6 meses debe ser resultado del balance entre las posibles consecuencias en la audición, el retraso del lenguaje, el desarrollo general y el rendimiento escolar.
Los tímpanos que han padecido durante mucho tiempo de otitis serosa o han sido sometidos a varias miringotomías tienen tendencia a la atrofia, pudiendo producirse una perforación timpánica, bolsas de retracción, otitis adhesiva o, incluso, desarrollar un colesteatoma.
El objetivo real del tratamiento es el control de la enfermedad y no su curación, ya que esta será proporcionada por el crecimiento y desarrollo o por el tratamiento de la causa de la obstrucción tubárica, y no por las estrategias médicas o quirúrgicas que empleemos.
Tratamiento médico
El tratamiento médico de la otitis serosa aguda (menos de tres semanas de duración) y subaguda (de tres semanas a tres meses) es controvertido, debido a la tendencia natural a la resolución espontánea de estos cuadros (que tiene lugar en el 80% de los casos).
La otitis serosa crónica, si bien es posible que se resuelva espontáneamente, muchas veces requiere tratamiento, ya sea médico o quirúrgico.
La profilaxis antibiótica ha sido empleada con éxito para disminuir los episodios de otitis media aguda, pero no son útiles en la prevención de la otitis media serosa.
El papel de la audiometría en el diagnóstico de los niños es limitado debido a la dificultad para su correcta colaboración, siendo necesario en ocasiones recurrir a audiometrías de juego o con reflejos condicionados.
Los antibióticos han demostrado un efecto moderado en el control de la otitis serosa a corto plazo, sin embargo su efectividad a largo plazo no ha sido demostrada. Además, diversos estudios indican que la efectividad del uso de antibióticos disminuye en los pacientes previamente tratados, por lo que en los niños que ya han recibido varios ciclos de antibióticos, resulta inútil prescribir uno nuevo.
Los efectos secundarios más frecuentes de la terapia antibiótica incluyen erupciones cutáneas, vómitos, diarrea y reacciones alérgicas, además de favorecer el desarrollo de resistencias bacterianas.
Los corticoides por vía sistémica asociados a la antibioterapia también han demostrado acelerar la resolución de la otitis (demuestran beneficio en uno de cada tres niños tratados), si bien la mayoría de los autores no justifican su uso, principalmente debido a sus efectos secundarios (cambios en el comportamiento, aumento del apetito, además de los efectos más graves como la supresión adrenal y la necrosis avascular de la cabeza del fémur). Los corticoides tópicos intranasales tienen menos efectos secundarios, sin embargo su uso no ofrece mejoría en el transcurso de dos semanas en el tratamiento asociado a antibióticos sobre la antibioterapia sola.
Los antihistamínicos y los descongestionantes nasales no han mostrado ningún beneficio respecto a placebo en varios estudios, por lo tanto, no se justifica su empleo en el tratamiento de forma sistemática. Para otras terapias utilizadas en el tratamiento de la otitis media, tales como la autoinsuflación de la trompa de Eustaquio, el uso oral o intratimpánico de mucolíticos y el uso de otros agentes farmacológicos distintos a antibióticos, esteroides, antihistamínicos y descongestionantes, no existe ninguna evidencia en la literatura disponible.
Tratamiento quirúrgico
La curación definitiva de este proceso depende de la resolución de la obstrucción tubárica, así como del crecimiento del cráneo y la maduración de la trompa de Eustaquio. El tratamiento quirúrgico persigue disminuir el número de episodios de otitis y evitar las complicaciones que pueden derivar de la ocupación crónica del oído, además de mejorar la audición de estos pacientes. Se debe indicar cirugía en pacientes con otitis serosas agudas de repetición de al menos cuatro episodios en seis meses.

El tratamiento depende de la edad del paciente, considerando la miringotomía, con o sin colocación de tubos de drenaje transtimpánicos, y la adenoidectomía como principales opciones cuando falla el tratamiento médico.
La miringotomía consiste en realizar una pequeña apertura en la membrana timpánica que permite el drenaje y aspirado del contenido del oído medio. Consigue equilibrar la presión del oído medio y resolver la hipoacusia de transmisión del paciente, además de reducir la tendencia a las infecciones de repetición. Sin embargo, no es efectiva por sí sola en el tratamiento de la otitis serosa a largo plazo, ya que el orificio se cierra en pocos días y la otitis puede recurrir en caso de persistencia de los mecanismos desencadenantes.
Algunos autores apoyan la miringotomía con láser, que consigue un orificio que se mantiene abierto durante más tiempo, pero se asocia a una mayor incidencia de perforaciones timpánicas permanentes.
Aproximadamente el 50% de los oídos con otitis serosa se normalizan en un período de dos meses, por lo que es recomendable esperar al menos tres meses antes de establecer un tratamiento quirúrgico.
La colocación de tubos de ventilación transtimpánicos permite la ventilación del oído medio durante períodos de tiempo más prolongados. Existen distintos tipos de drenajes, los temporales, que suelen mantenerse una media de 6-12 meses y que suelen extruirse de forma espontánea, y los permanentes (tubos en T), indicados en aquellos pacientes en que es precisa la colocación de varios drenajes consecutivos por recurrencia de la clínica.

La complicación más frecuente de los drenajes es la otorrea, resultado del reflujo de secreciones desde la nasofaringe o por el desarrollo de una OMA secundaria a la entrada de agua contaminada en el oído medio a través del drenaje.
Se considera que a menor longitud del tubo de drenaje, es más probable la extrusión precoz del mismo, y a mayor longitud, existe un mayor riesgo de perforación timpánica permanente (hasta el 2% en los drenajes temporales y 17% en los permanentes).
La adenoidectomía es la cirugía mayor más utilizada en la prevención de las otitis medias. Por si sola o asociada a miringotomía, consigue disminuir la incidencia y la duración de la otitis serosa, y el número de episodios de otitis media aguda, independientemente del tamaño de las adenoides, ya que mejora la ventilación de la trompa de Eustaquio, permitiendo un adecuado equilibrio de presiones. Sin embargo, no es un procedimiento exento de complicaciones por lo que debe estudiarse de forma independiente su indicación en cada caso.
La amigdalectomía no está indicada, por sí sola, en el tratamiento de la otitis serosa.
Tratamiento de la otitis seromucosa en adultos
El tratamiento en adultos, al igual que en los niños, debe ir encaminado a resolver el proceso causal de la otitis, restableciendo un equilibrio de presiones en el oído medio y favoreciendo el drenaje de secreciones. Las medidas terapéuticas disponibles en adultos son las mismas que en la edad pediátrica, teniendo siempre presente que la curación espontánea es menos frecuente que en los niños.
Inicialmente instauraremos un tratamiento médico encaminado a mejorar la ventilación tubárica, con lavados nasales, asociado a un corticoide tópico nasal y, en ocasiones, un ciclo corto de aerosolterapia.
Aquellos casos en los que la otitis serosa acompaña a un cuadro agudo o crónico de sinusitis, el tratamiento será el mismo para ambos procesos añadiendo un ciclo de antibioterapia. En caso de persistencia de moco en oído medio a pesar del tratamiento médico, debemos plantear la miringotomía, con o sin colocación de drenaje transtimpánico, en función de la etiología.
En los casos en que sospechemos que el origen de la otitis se debe a una obstrucción nasal por poliposis nasosinusal, una sinusitis crónica que no responde al tratamiento médico inicial o en caso de dismorfia septal severa, se debe recomendar tratamiento quirúrgico de la misma.
Un grupo especial lo constituyen los pacientes con patología maligna en la nasofaringe. En estos, el desarrollo de una otitis serosa es el resultado de un conjunto de alteraciones producidas tanto por el tumor, como por los tratamientos empleados, en especial la radioterapia, que no solo afecta al funcionamiento de la trompa, sino que altera la mucosa del oído medio, cambia las propiedades del moco y disminuye su eliminación. En estos pacientes, el tratamiento más efectivo y con menos índice de complicaciones consiste en repetidas miringotomías con aspirado del contenido mucoso. Se debe evitar la colocación de tubos de drenaje que se asocian a una peor evolución, con otorreas frecuentes y una mayor pérdida auditiva, tanto transmisiva como neurosensorial.

El tratamiento inicial se basará en medidas de higiene local y solo se recurrirá a la cirugía en caso de persistencia de la otitis, en presencia de complicaciones o en pacientes de riesgo.
| TRATAMIENTO DE LA OTITIS SEROSA | |
|---|---|
| Efectividad probada | Abstención terapéutica. Miringotomía con o sin colocación de tubos de drenaje. Antibióticos. Corticoides sistémicos o tópicos. Tratamiento de enfermedades desencadenantes. |
| Efectividad dudosa / nula | Descongestionantes nasales. Antihistamínicos. Mucolíticos. Amigdalectomía. |
Opciones de tratamiento.
Puntos clave
En niños y adultos, el diagnóstico se basa en la historia clínica y en la exploración física mediante otoscopia.
Dada la fisiopatología de la otitis serosa, la exploración de la vía aérea superior en busca de factores predisponentes resulta imprescindible.
El tratamiento debe ir encaminado a restablecer el equilibrio de presiones del oído medio con la nasofaringe.
El tratamiento inicial será conservador, fundamentalmente mediante medidas de higiene local, y solo se recurrirá a la cirugía en caso de persistencia de la otitis, en presencia de complicaciones o en pacientes de riesgo.
Es imprescindible el tratamiento del proceso desencadenante de la otitis para evitar recurrencias.
Nunca debemos olvidar en los adultos descartar la presencia de un tumor en nasofaringe ante el desarrollo de una otitis serosa unilateral.